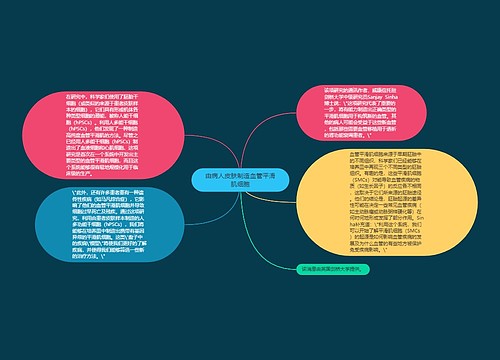
首次鉴定出新血管形成的关键性蛋白Raf-1思维导图
空城旧人
2023-02-21

芽生式血管生成(angiogenic sprouting),即一从现有血管长出新血管的过程,是一把双刃剑。它能够让胚胎长出心血管系统,同时对于成年人组织再生也是至关重要的。但是它也给生长中的肿瘤供给营养物和氧气。
树图思维导图提供《首次鉴定出新血管形成的关键性蛋白Raf-1》在线思维导图免费制作,点击“编辑”按钮,可对《首次鉴定出新血管形成的关键性蛋白Raf-1》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:82304f3d1955cb4376e71a2db2e216c7
思维导图大纲
相关思维导图模版
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

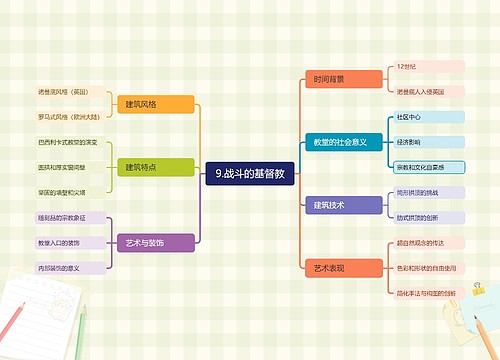
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a