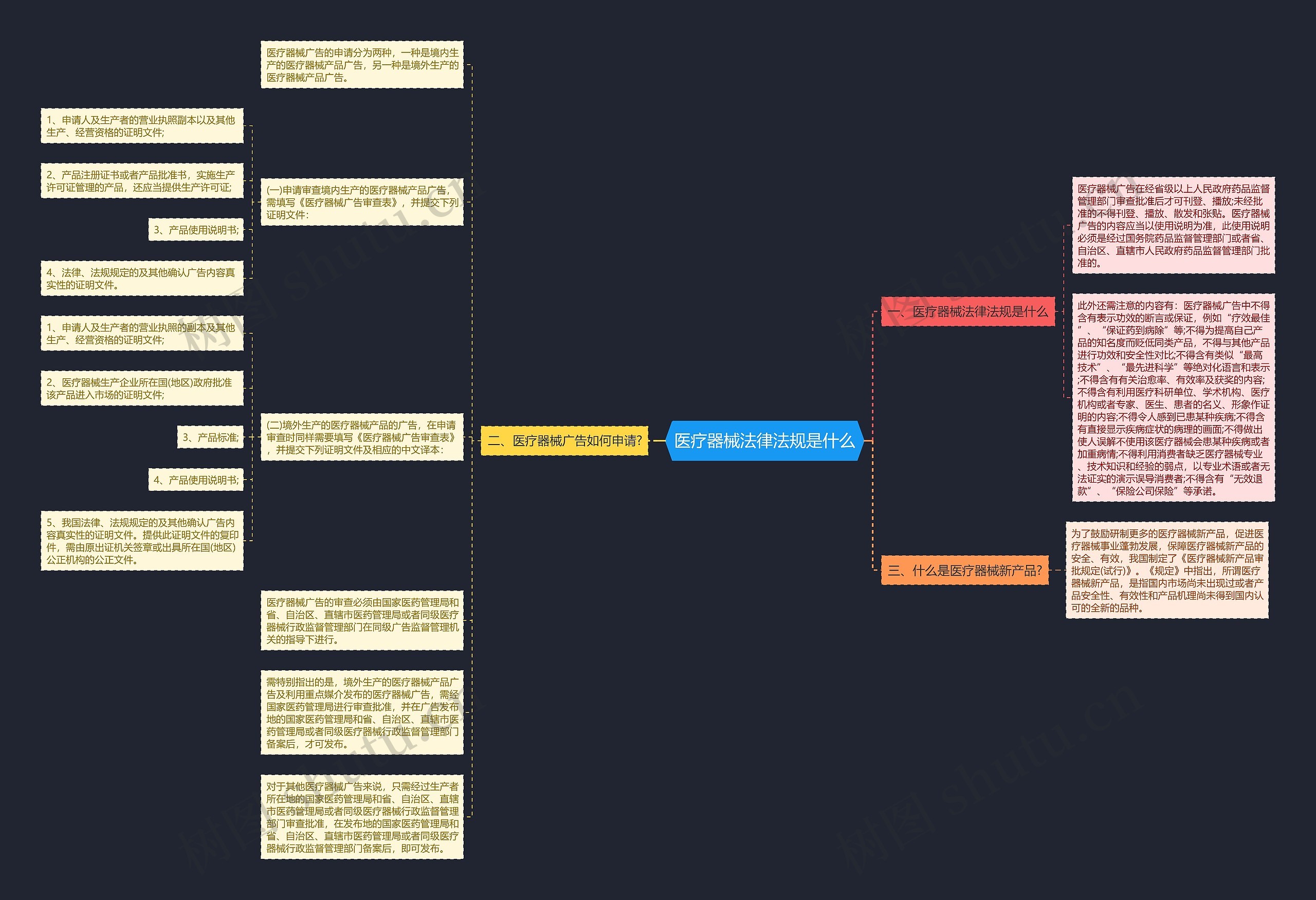
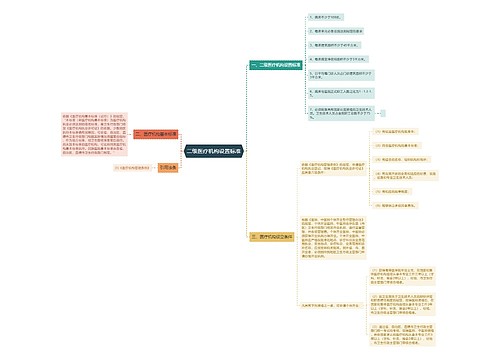
医疗器械广告的申请分为两种,一种是境内生产的医疗器械产品广告,另一种是境外生产的医疗器械产品广告。
(一)申请审查境内生产的医疗器械产品广告,需填写《医疗器械广告审查表》,并提交下列证明文件:
1、申请人及生产者的营业执照副本以及其他生产、经营资格的证明文件;
2、产品注册证书或者产品批准书,实施生产许可证管理的产品,还应当提供生产许可证;
4、法律、法规规定的及其他确认广告内容真实性的证明文件。
(二)境外生产的医疗器械产品的广告,在申请审查时同样需要填写《医疗器械广告审查表》,并提交下列证明文件及相应的中文译本:
1、申请人及生产者的营业执照的副本及其他生产、经营资格的证明文件;
2、医疗器械生产企业所在国(地区)政府批准该产品进入市场的证明文件;
5、我国法律、法规规定的及其他确认广告内容真实性的证明文件。提供此证明文件的复印件,需由原出证机关签章或出具所在国(地区)公正机构的公正文件。
医疗器械广告的审查必须由国家医药管理局和省、自治区、直辖市医药管理局或者同级医疗器械行政监督管理部门在同级广告监督管理机关的指导下进行。
需特别指出的是,境外生产的医疗器械产品广告及利用重点媒介发布的医疗器械广告,需经国家医药管理局进行审查批准,并在广告发布地的国家医药管理局和省、自治区、直辖市医药管理局或者同级医疗器械行政监督管理部门备案后,才可发布。
对于其他医疗器械广告来说,只需经过生产者所在地的国家医药管理局和省、自治区、直辖市医药管理局或者同级医疗器械行政监督管理部门审查批准,在发布地的国家医药管理局和省、自治区、直辖市医药管理局或者同级医疗器械行政监督管理部门备案后,即可发布。