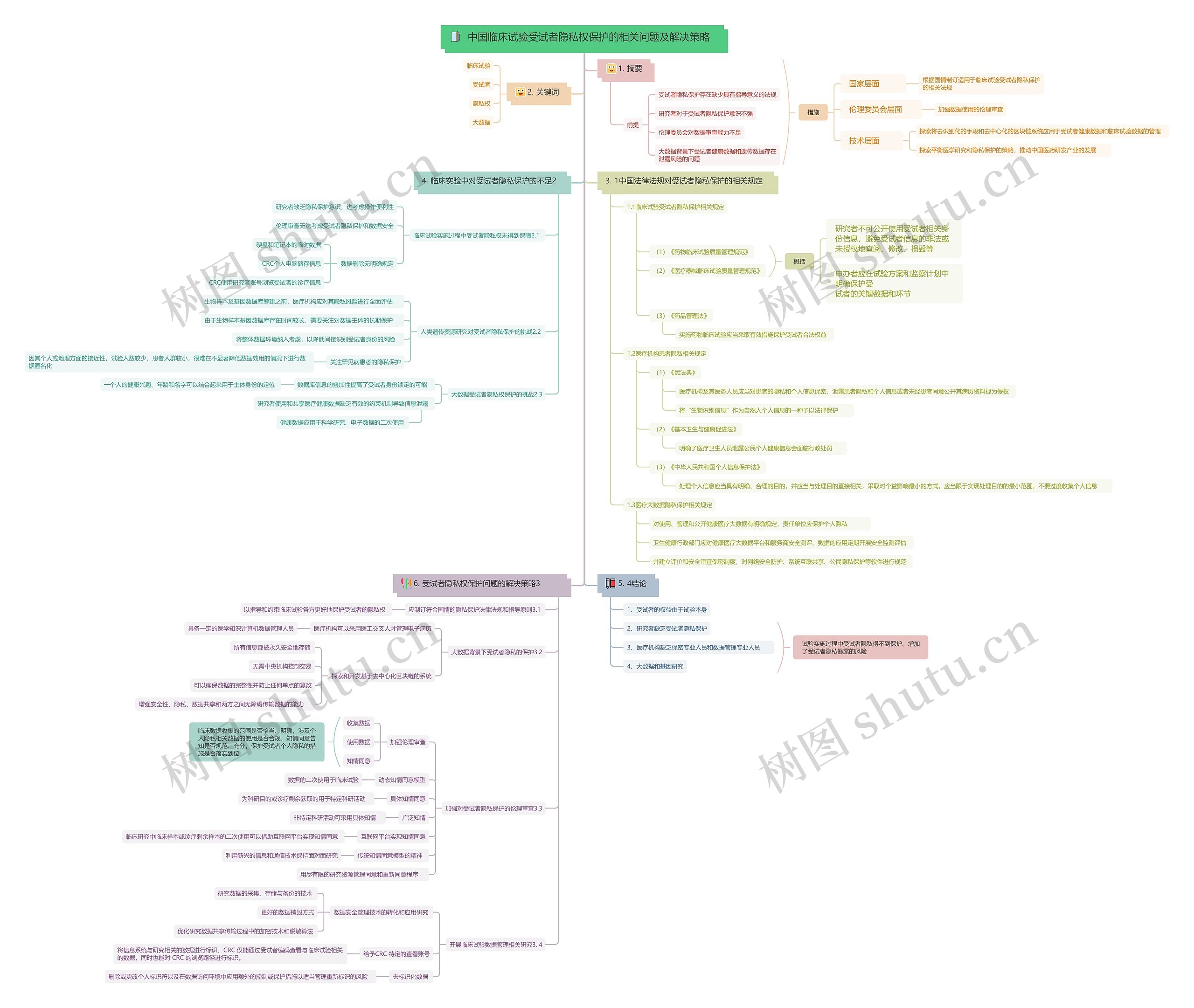
中国临床试验受试者隐私权保护的相关问题及解决策略思维导图模板大纲
摘要
前提
大数据背景下受试者健康数据和遗传数据存在泄露风险的问题
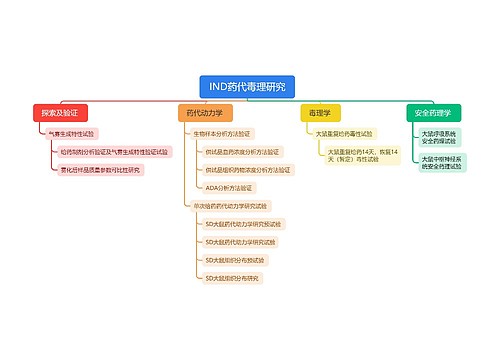
1中国法律法规对受试者隐私保护的相关规定
1.1临床试验受试者隐私保护相关规定
(3)《药品管理法》
实施药物临床试验应当采取有效措施保护受试者
合法权益
1.2医疗机构患者隐私相关规定
(1)《民法典》
医疗机构及其医务人员应当对患者的隐私和个人信息保密,泄露患者隐私和个人信息或者未经患者同意公开其病历资料视为侵权
将“生物识别信息”作为自然
人个人信息的一种予以法律保护
(2)《基本卫生与健康促进法》
明确了医疗卫生人员泄露公民个人健康信息会面临行政处罚
(3)《中华人民共和国个人信息保护法》
处理个人信息应当具有明确、合理的目的,并应
当与处理目的直接相关,采取对个益影响最小的
方式,应当限于实现处理目的的最小范围,不要过度收集个人信息
1.3医疗大数据隐私保护相关规定
对使用、管理和公开健康医疗大数据有明确规定,责任单位应保护个人隐私
卫生健康行政部门应对健康医疗大数据平台和服务商安全测评、数据的应用定期开展安全监测评估
并建立评价和安全审查保密制度,对网络安全防护、系统互联共享、公民隐私保护等软件进行规范
临床实验中对受试者隐私保护的不足2
人类遗传资源研究对受试者隐私保护的挑战2.2
生物样本及基因数据库筹建之前,医
疗机构应对其隐私风险进行全面评估
由于生物样本基因数据库存在时间较长,需要关注对数据主体的长期保护
将整体数据环境纳入考虑,
以降低间接识别受试者身份的风险
关注罕见病患者的隐私保护
因其个人或地理方面的接近
性,试验人数较少,患者人群较小,很难在不显著降低
数据效用的情况下进行数据匿名化
大数据受试者隐私权保护的挑战2.3
数据库信
息的叠加性提高了受试者身份锁定的可能
一个
人的健康兴趣、年龄和名字可以结合起来用于主体身
份的定位
研究者使用和共享医疗健康数据缺乏有效的约束机制导致信息泄露
受试者隐私权保护问题的解决策略3
大数据背景下受试者隐私的保护3.2
探索和开发基于去中心化区块链的系统
增强安全性、隐私、数据共享和两方之间无障碍传输数据的能力
加强对受试者隐私保护的伦理审查3.3
互联网平台实现知情同意
临床研究中临床样本或诊疗剩余样本的二次使用可以借助互联网平台实现知情同意
开展临床试验数据管理相关研究3. 4
给予CRC 特定的查看账号
将信息系统与研究相关的数据进行标识,CRC 仅能通过受试者编码查看与临床试验相关的数据,同时也能对 CRC 的浏览路径进行标识。
去标识化数据
删除或更改个人标识符以及在数据访问环境中应用额外的控制或保护措施以适当管理重新标识的风险
试验实施过程中受试者隐私得不到保护、增加了受试者隐私暴露的风险思维导图模板大纲
措施思维导图模板大纲
国家层面
根据国情制订
适用于临床试验受试者隐私保护的相关法规
技术层面
探索将去识别化的手段和去中心化的区块链系统应用于受试者健康数据和临床试验数据的管理
探索平衡
医学研究和隐私保护的策略,推动中国医药研发产业的发展
概括思维导图模板大纲
研究者不可公开使用受试者相关身份信息,避免受试者信息的非法或未授权地查阅、修改、损毁等
申办者应在试验方案和监察计划中明确保护受
试者的关键数据和环节
临床数据收集的范围是否恰当、明确,涉及个人隐私相关数据的使用是否合规,知情同意告知是否规范、充分,保护受试者个人隐私的措施是否落实到位思维导图模板大纲
 U633687664
U633687664
 U782682106
U782682106