临床试验流程思维导图
divlo_
2022-11-13
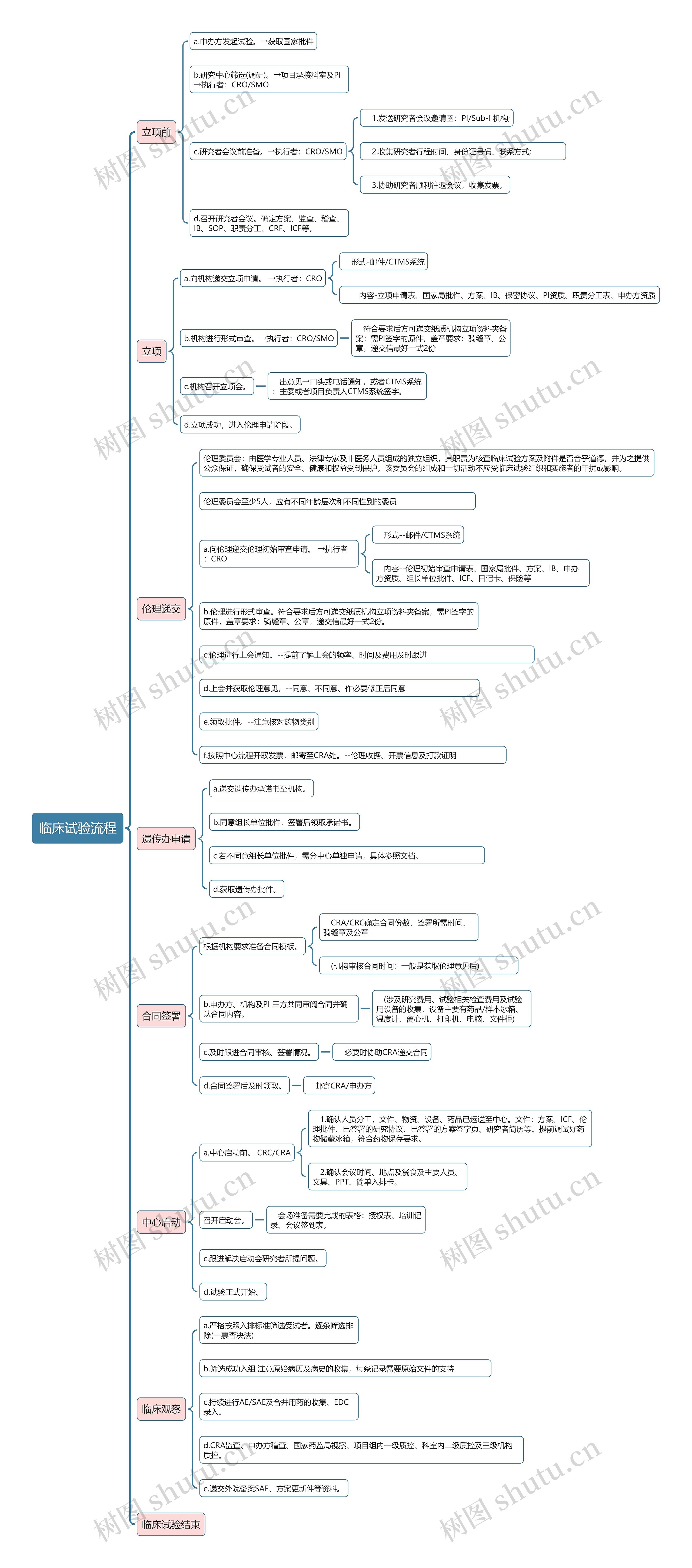
立项前 2.立项 3.伦理 4.遗传办 5.合同 6.中心启动 7.临床观察 8.临床试验结束
树图思维导图提供《临床试验流程》在线思维导图免费制作,点击“编辑”按钮,可对《临床试验流程》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a5b501cff63552a37553372f537fe5ef

立项前 2.立项 3.伦理 4.遗传办 5.合同 6.中心启动 7.临床观察 8.临床试验结束
树图思维导图提供《临床试验流程》在线思维导图免费制作,点击“编辑”按钮,可对《临床试验流程》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a5b501cff63552a37553372f537fe5ef