2010版《中国药典》8月定稿 药用辅料标准趋严思维导图
花房姑娘
2023-02-21

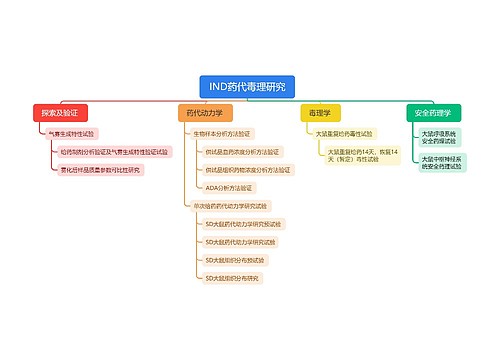
据相关人士透漏,按照计划,2010年版《中国药典》将在8月底完成全部科研任务和定稿工作,药用辅料标准的修订也在紧张进行当中。 新版药典关于辅料标准的修订工作即将完成,估计最终将收录辅料品种138种。目前已经完成公示二稿,8月底将完成定稿。
树图思维导图提供《2010版《中国药典》8月定稿 药用辅料标准趋严》在线思维导图免费制作,点击“编辑”按钮,可对《2010版《中国药典》8月定稿 药用辅料标准趋严》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:39fb259108a0f2ea7a5d3215b94ea28d
思维导图大纲
相关思维导图模版
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

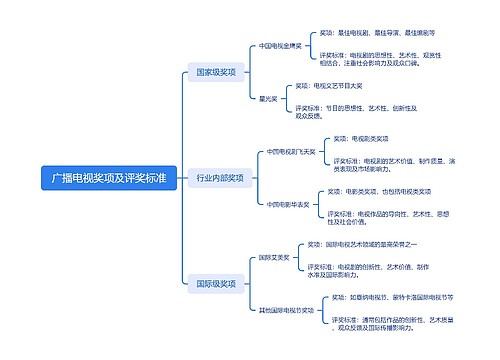
广播电视奖项及评奖标准思维导图
 U782682106
U782682106树图思维导图提供《广播电视奖项及评奖标准》在线思维导图免费制作,点击“编辑”按钮,可对《广播电视奖项及评奖标准》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a4210651fa3a78355ac9f5101bb2c616