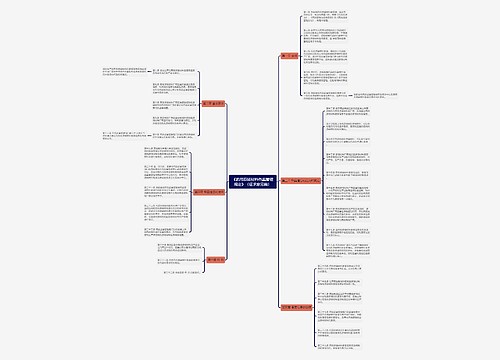
医疗机构药品质量监督管理办法(征求意见稿)思维导图
清风和酒
2023-02-21

第一章 总 则 第一条(立法目的及依据) 为配合医药卫生体制改革,积极推进国家基本药物制度,加强医疗机构药品质量监督管理,保障人体用药安全、有效、合理,根据《中华人民共和国药品管理法》(以下简称《药品管理法》)以及《中华人民共和国药品管理法实施条例》(以下简称《药品管理法实施条例》)医`学教育
树图思维导图提供《医疗机构药品质量监督管理办法(征求意见稿)》在线思维导图免费制作,点击“编辑”按钮,可对《医疗机构药品质量监督管理办法(征求意见稿)》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:6893257536780604bfa7eaa7918c1ea1
思维导图大纲
相关思维导图模版
业务查询耗时质量问题思维导图
 U250722818
U250722818树图思维导图提供《业务查询耗时质量问题》在线思维导图免费制作,点击“编辑”按钮,可对《业务查询耗时质量问题》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:b79e68d755ecdc53367789daeec4d579
全面准确把握“一取消三不再”的主旨要义思维导图
 U453440030
U453440030树图思维导图提供《全面准确把握“一取消三不再”的主旨要义》在线思维导图免费制作,点击“编辑”按钮,可对《全面准确把握“一取消三不再”的主旨要义》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:f37eda4c07aeeae84605a7a15a5a2ec1