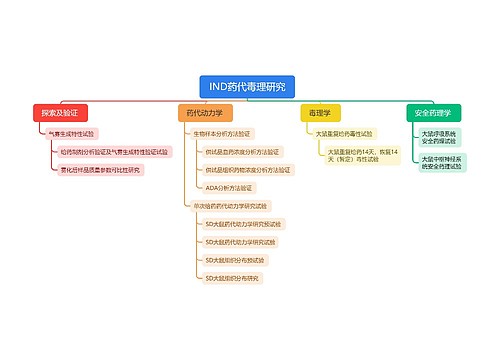
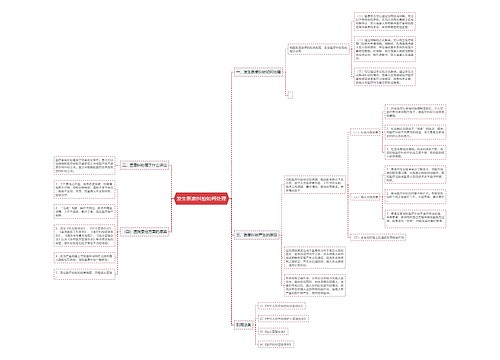
临床试验试验方案思维导图
回憶褶皺
2023-02-21

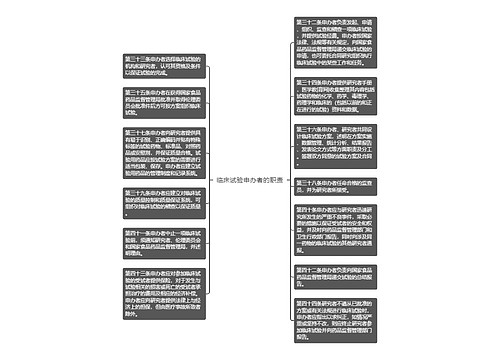
第十六条临床试验开始前应制定试验方案,该方案应由研究者与申办者共同商定并签字,报伦理委员会审批后实施。
树图思维导图提供《临床试验试验方案》在线思维导图免费制作,点击“编辑”按钮,可对《临床试验试验方案》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:b9befa09ec3a45cee98fb98cba90164f
思维导图大纲
相关思维导图模版
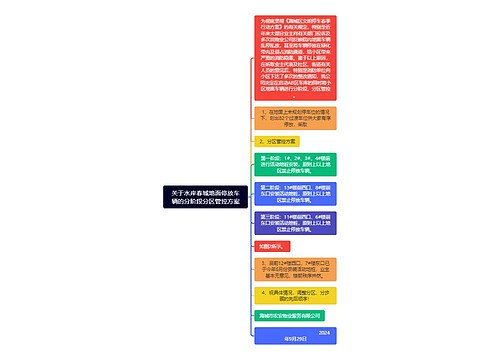
关于水岸春城地面停放车辆的分阶段分区管控方案思维导图
 U882214155
U882214155树图思维导图提供《关于水岸春城地面停放车辆的分阶段分区管控方案》在线思维导图免费制作,点击“编辑”按钮,可对《关于水岸春城地面停放车辆的分阶段分区管控方案》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:b7cacbcb60cd785d3e836665ab120d6d
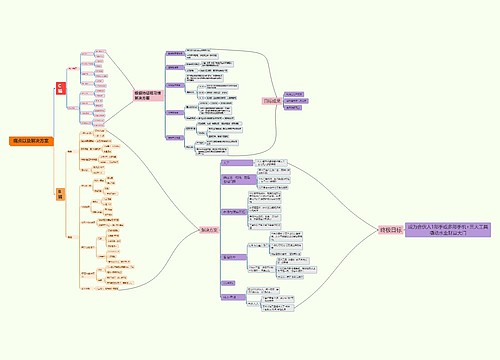
痛点以及解决方案思维导图
 U381309528
U381309528树图思维导图提供《痛点以及解决方案》在线思维导图免费制作,点击“编辑”按钮,可对《痛点以及解决方案》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:3e3e2559b67426956361b028cbc57f36