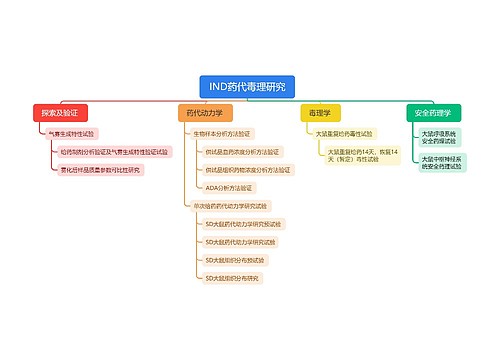
核发《药品生产企业许可证》验收标准(暂行)思维导图
微风不燥
2023-02-21

根据《药品管理法》第二章的规定和《药品管理法实施办法》第三章、第六章的规定,参照《药品生产质量管理规范》的规定,制定本验收标准。
树图思维导图提供《核发《药品生产企业许可证》验收标准(暂行)》在线思维导图免费制作,点击“编辑”按钮,可对《核发《药品生产企业许可证》验收标准(暂行)》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:95ec32d1e5953809d78f555cdfea0b67
思维导图大纲
相关思维导图模版
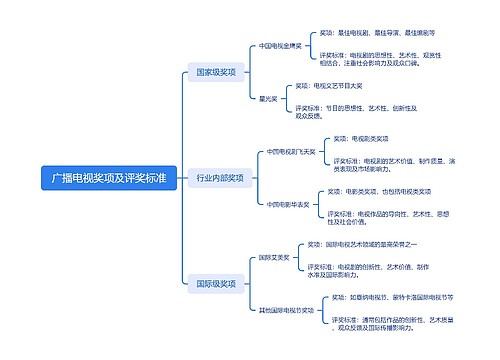
广播电视奖项及评奖标准思维导图
 U782682106
U782682106树图思维导图提供《广播电视奖项及评奖标准》在线思维导图免费制作,点击“编辑”按钮,可对《广播电视奖项及评奖标准》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a4210651fa3a78355ac9f5101bb2c616
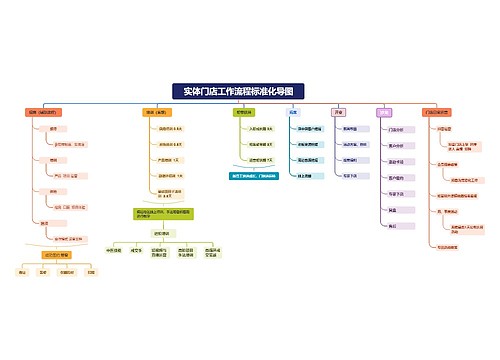
实体门店工作流程标准化导图思维导图
 U981878554
U981878554树图思维导图提供《实体门店工作流程标准化导图》在线思维导图免费制作,点击“编辑”按钮,可对《实体门店工作流程标准化导图》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:1a305a94ffb852ebf3c1ddc1da6184b7