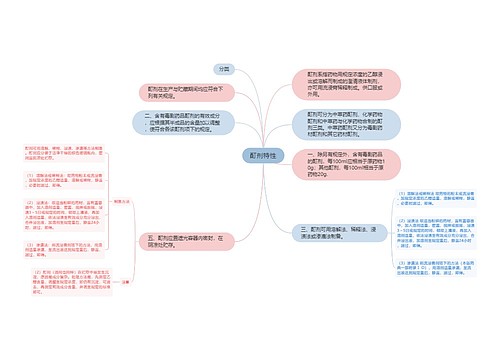
注射剂系指药物制成的供注入体内的灭菌溶液、乳状液或混悬液,以及供临用前配成溶液或混悬液的无菌粉末或浓溶液。
注射剂的类型与要求,除一般小剂量溶液型注射剂以外,尚有以下类型。
注射用混悬液:除另有规定外,药物的粒度应控制在15μm以下,含15~20μm(间有个别20~50μm)者不应超过10%.注射用混悬液不得用于静脉注射与椎管注射。
注射用无菌粉末:供直接分装成注射用无菌粉末的原料药应无菌。凡用冷冻干燥法制备,其药液应无菌,灌装时装量差异应控制在规定限度以内。标签上应有用前配制方法说明。
一、溶剂:注射剂所用的溶剂包括水性溶剂、植物油及其他非水性溶剂等。最常用的水性溶剂为注射用水,亦可用0.9%氯化钠溶液或其他适宜的水溶液。非水溶剂有乙醇、丙二醇、聚乙二醇的水溶液。
常用的油溶剂为注射用大豆油。其质量应符合大豆油(供注射用)的标准。
抑菌剂用量应能抑制注射液内微生物的生长。加有抑菌剂的注射液,仍应用适宜的方法灭菌。
注射量超过5ml的注射液,添加的抑菌剂必须特别审慎选择。供静脉(除另有规定外)或椎管注射用的注射液,均不得添加抑菌剂。
三、容器:注射剂常用容器有玻璃安瓿、玻璃瓶、塑料瓶等,容器除另有规定外,应符合国家标准中有关药用玻璃容器和塑料容器的规定。容器胶塞亦应符合有关规定。
四、配制:注射液的配制应遵守有关规程,容器应洁净干燥后使用。
注射剂在配制过程中,应严密防止微生物与热原的污染及药物的变质。已调配的药液应在当日内完成灌封、灭菌,如不能在当日内完成,必须将药液在不变质与不易繁殖微生物的条件下保存;供静脉及椎管注射者,更应严格控制。
五、灌装:接触空气易变质的药物,在灌装过程中,容器内应排除空气,填充二氧化碳或氮等气体后熔封。
六、熔封或严封:熔封或严封后,可根据药物性质选用适宜的方法灭菌,但必须保证制成品无菌。
七、检漏:熔封的注射剂在灭菌时或灭菌后,应采用减压法或其他适宜的方法进行容器检漏。
八、贮存:注射剂除应遮光贮存外,并应按规定的条件贮存。
50:1.0:1.5
检查法注射液的标示装量为2ml或2ml以下者取供试品5支,2ml以上至10ml者取供试品3支,10ml以上者取供试品2支;开启时注意避免损失,将内容物分别用相应体积的干燥注射器及注射针头抽尽,然后注入标化的量具内,在室温下检视;测定油溶液或混悬液的装量时,应先加温摇匀,再用干燥注射器及注射针头抽尽后,同前法操作,放冷至室温检视,每支注射液的装量均不得少于其标示量。
注射液的标示装量为50ml以上至500ml的按最低装量检查法(附录Ⅹ:F)检查,应符合规定。
0.50g以上:±5%
检查法取供试品5瓶(支),除去标签、铝盖,容器外壁用乙醇洗净,干燥,开启时注意避免玻璃屑等异物落入容器中,分别迅速精密称定,倾出内容物,容器可用水、乙醇洗净,在适宜条件下干燥后,再分别精密称定每一容器的重量,求出每1瓶(支)的装量与平均装量。每1瓶(支)中的装量与平均装量相比较,应符合左表的规定,如有1瓶(支)不符合,应另取10瓶(支)复试,均符合规定。

 U633687664
U633687664
 U582679646
U582679646