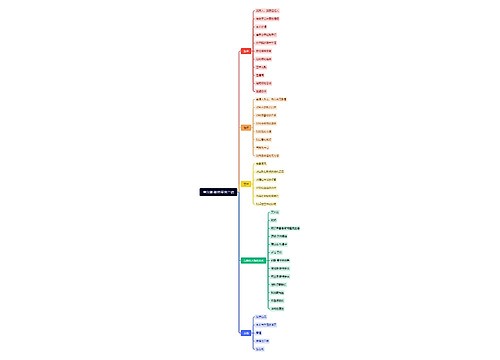
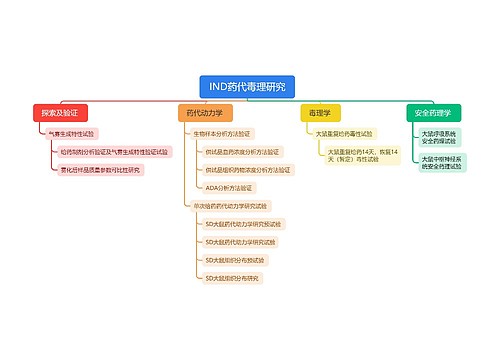
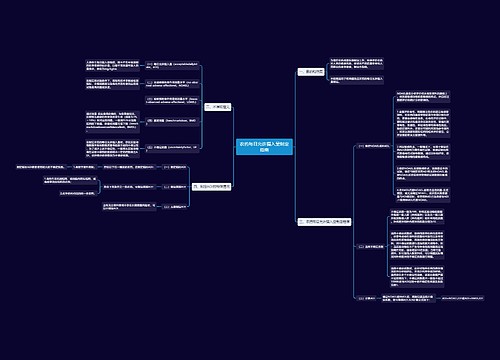
保健食品注册检验复核检验规范思维导图
微笑感染人
2023-02-20

【发布单位】 国家食品药品监督管理局 【发布文号】 国食药监许(2011)173号 【发布日期】 2011-04-11 【生效日期】 2011-04-11 各省、自治区、直辖市食品药品监督管理局(药品监督管理局),有关单位: 现将《保健食品注册检验复核检验管理办法》和《保健食品注册检验复核检验规范》印发给你们,请遵照执行。
树图思维导图提供《保健食品注册检验复核检验规范》在线思维导图免费制作,点击“编辑”按钮,可对《保健食品注册检验复核检验规范》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:11a7015009b9311e77e6528c32f00a6f
思维导图大纲
相关思维导图模版
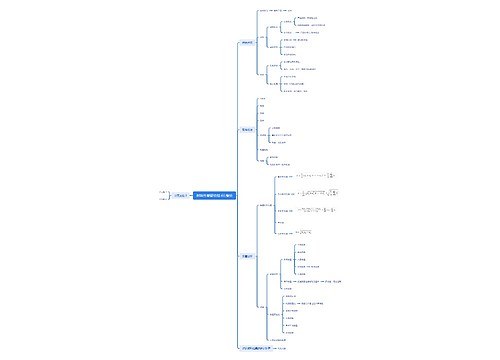
材料性能研究技术I 绪论思维导图
 U360192672
U360192672树图思维导图提供《材料性能研究技术I 绪论》在线思维导图免费制作,点击“编辑”按钮,可对《材料性能研究技术I 绪论》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:998f596fb2e786e87c5f6612ff0356e1
查尔斯·斯特里克兰德思维导图
 U866779029
U866779029树图思维导图提供《查尔斯·斯特里克兰德》在线思维导图免费制作,点击“编辑”按钮,可对《查尔斯·斯特里克兰德》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:dcc23eab5e1456239090318fd2a36733