卫生部人类辅助生殖技术与人类精子库校验实施细则思维导图
时光静好
2023-02-20

为切实、有效实施《人类辅助生殖技术管理办法》和《人类精子库管理办法》(以下简称两个《办法》),严格执行《人类辅助生殖技术规范》、《人类精子库基本标准与技术规范》和《人类辅助生殖技术与人类精子库的伦理原则》(以下简称《技术规范、基本标准和伦理原则》)等文件,确保上述技术规范的应用与有序发展,不断完善动
树图思维导图提供《卫生部人类辅助生殖技术与人类精子库校验实施细则》在线思维导图免费制作,点击“编辑”按钮,可对《卫生部人类辅助生殖技术与人类精子库校验实施细则》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:f0c167a3a17dcbe463f7b9293262525f
思维导图大纲
相关思维导图模版
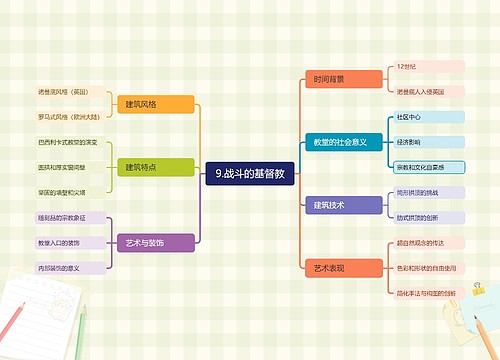
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a
第六章 群体传播与组织传播_副本思维导图
 U882673919
U882673919树图思维导图提供《第六章 群体传播与组织传播_副本》在线思维导图免费制作,点击“编辑”按钮,可对《第六章 群体传播与组织传播_副本》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:1672f555831e7d9a3bb2cf2fb792cb49