体外诊断试剂注册变更要求思维导图
谁相伴
2023-02-20
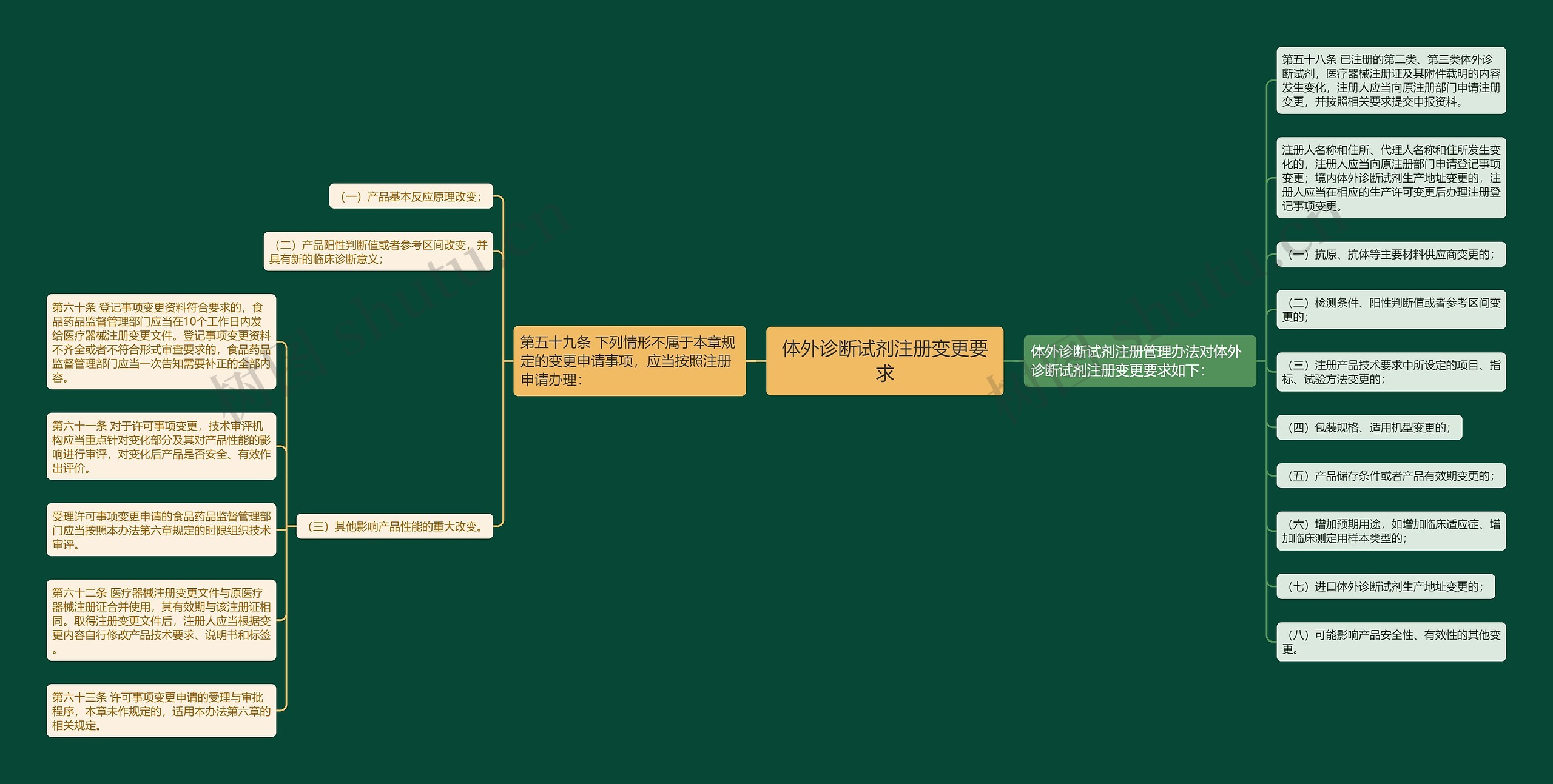
体外诊断试剂注册管理办法对体外诊断试剂注册变更要求如下: 第五十八条 已注册的第二类、第三类体外诊断试剂,医疗器械注册证及其附件载明的内容发生变化,注册人应当向原注册部门申请注册变更,并按照相关要求提交申报资料。
树图思维导图提供《体外诊断试剂注册变更要求》在线思维导图免费制作,点击“编辑”按钮,可对《体外诊断试剂注册变更要求》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:88c21539a5411d167251dadd21cb6073
思维导图大纲
相关思维导图模版
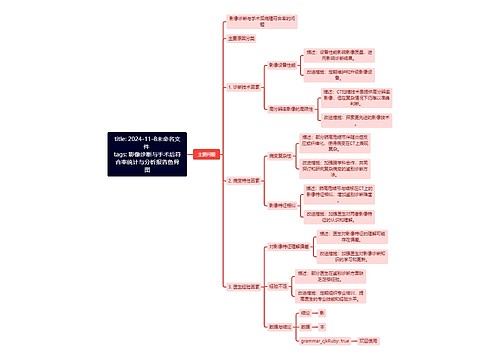
title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图思维导图
 U880271396
U880271396树图思维导图提供《title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图》在线思维导图免费制作,点击“编辑”按钮,可对《title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:f19c198bf7435acf7735ee5051a89d7b
卫生化学--元素和无机物分析思维导图
 U882044555
U882044555树图思维导图提供《卫生化学--元素和无机物分析》在线思维导图免费制作,点击“编辑”按钮,可对《卫生化学--元素和无机物分析》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4c942d0350c858e06a1f7ed29a86d096