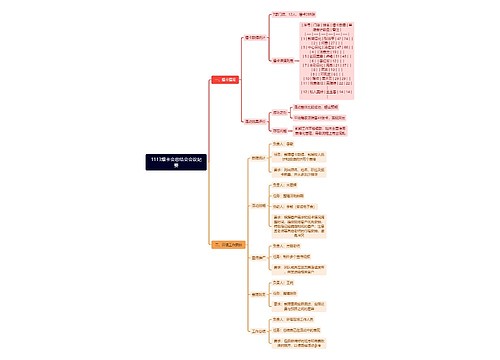
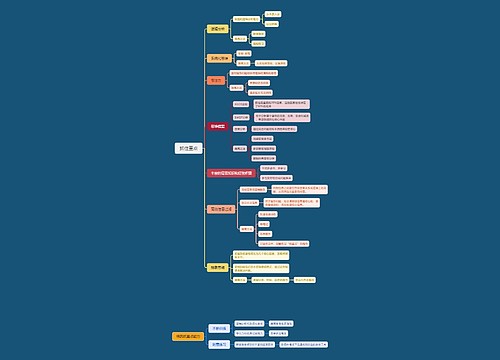
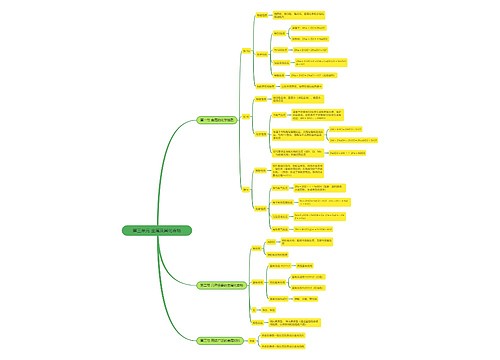
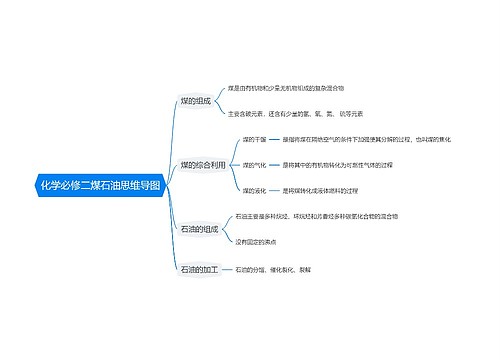
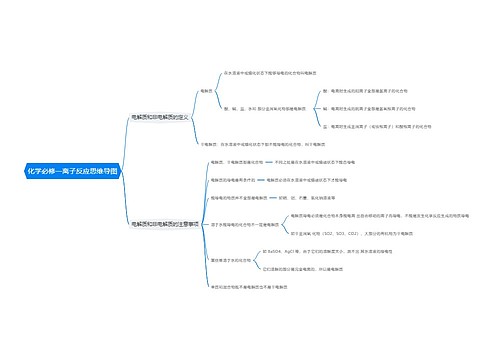
离子反应中,不可以拆开的物质有:单质、气体、沉淀、水、弱酸、弱碱、氧化物及绝大部分有机物(有机盐除外),由于发生复分解反应,离子不能大量共存
(1)有气体产生。例如:CO3、SO3、S、HCO3、HSO3、HS等易挥发的弱酸的酸根与H+不能大量共存。
(2)有沉淀生成。例如:Ba、Ca、Mg、Ag等不能与SO4、CO3等大量共存;Mg、Fe、Ag、Al、Zn、Cu、Fe等不能与OH大量共存;Pb与Cl,Fe与S、Ca2与PO4、Ag与Cl、Br、I等不能大量共存。
(3)有弱电解质生成。例如:OH﹣、CH3COO﹣、PO43﹣、HPO42﹣、H2PO4﹣、F、ClO﹣、AlO、SiO32﹣、CN、C17H35COO、等与H﹢不能大量共存;一些酸式弱酸根,例如:HCO3﹣、HPO42﹣、HS、H2PO4﹣、HSO3不能与OH﹣大量共存;NH4与OH不能大量共存。
(4)一些容易发生水解的离子,在溶液中的存在是有条件的:
① 例如:AlO2、S2﹣、CO32﹣、C6H5O等必须在碱性条件下才能在溶液中存在;
②再如:Fe2﹢、Al3﹢等必须在酸性条件下才能在溶液中存在。
这两类离子不能同时存在在同一溶液中,即离子间能发生“双水解”反应。
例如:3AlO2﹣十Al3﹢十6H2O=4Al(OH)3↓等
典型双水解的条件;弱酸根、弱碱根离子对应的酸碱容易从体系中脱离。即生成沉淀、气体或同时生成两种沉淀