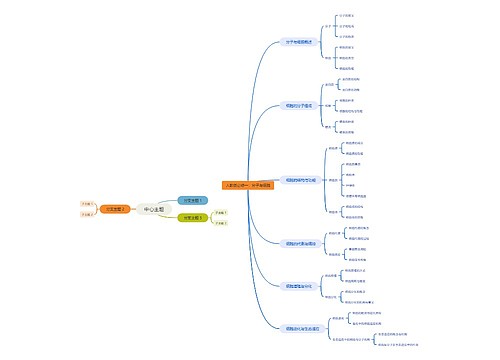
物理性质:黄绿色气体,有刺激性气味、可溶于水、加压和降温条件下可变为液态液氯和固态。
制法:MnO2+4HCl浓MnCl2+2H2O+Cl2
化学性质:很活泼,有毒,有氧化性,能与大多数金属化合生成金属氯化物盐。也能与非金属反应:
2Na+Cl2===点燃2NaCl2Fe+3Cl2===点燃2FeCl3Cu+Cl2===点燃CuCl2
Cl2+H2===点燃2HCl现象:发出苍白色火焰,生成大量白雾。
燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧。
①自来水杀菌消毒Cl2+H2O==HCl+HClO2HClO===光照2HCl+O2↑
1体积的水溶解2体积的氯气形成的溶液为氯水,为浅黄绿色。其中次氯酸HClO有强氧化性和漂泊性,起主要的消毒漂白作用。次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效。
制漂白液Cl2+2NaOH=NaCl+NaClO+H2O,其有效成分NaClO比HClO稳定多,可长期存放制漂白粉有效氯35%和漂粉精充分反应有效氯70%2Cl2+2CaOH2=CaCl2+CaClO2+2H2O
⑤有机化工:合成塑料、橡胶、人造纤维、农药、染料和药品