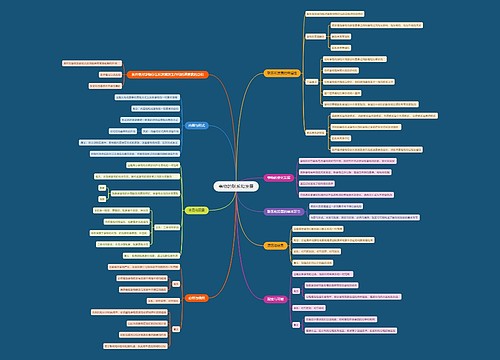
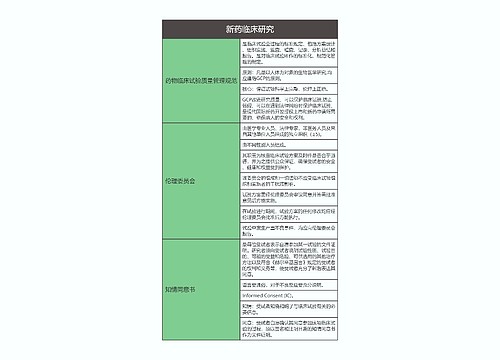
药理学 研究者、申办者与监查员思维导图
。
2022-10-28
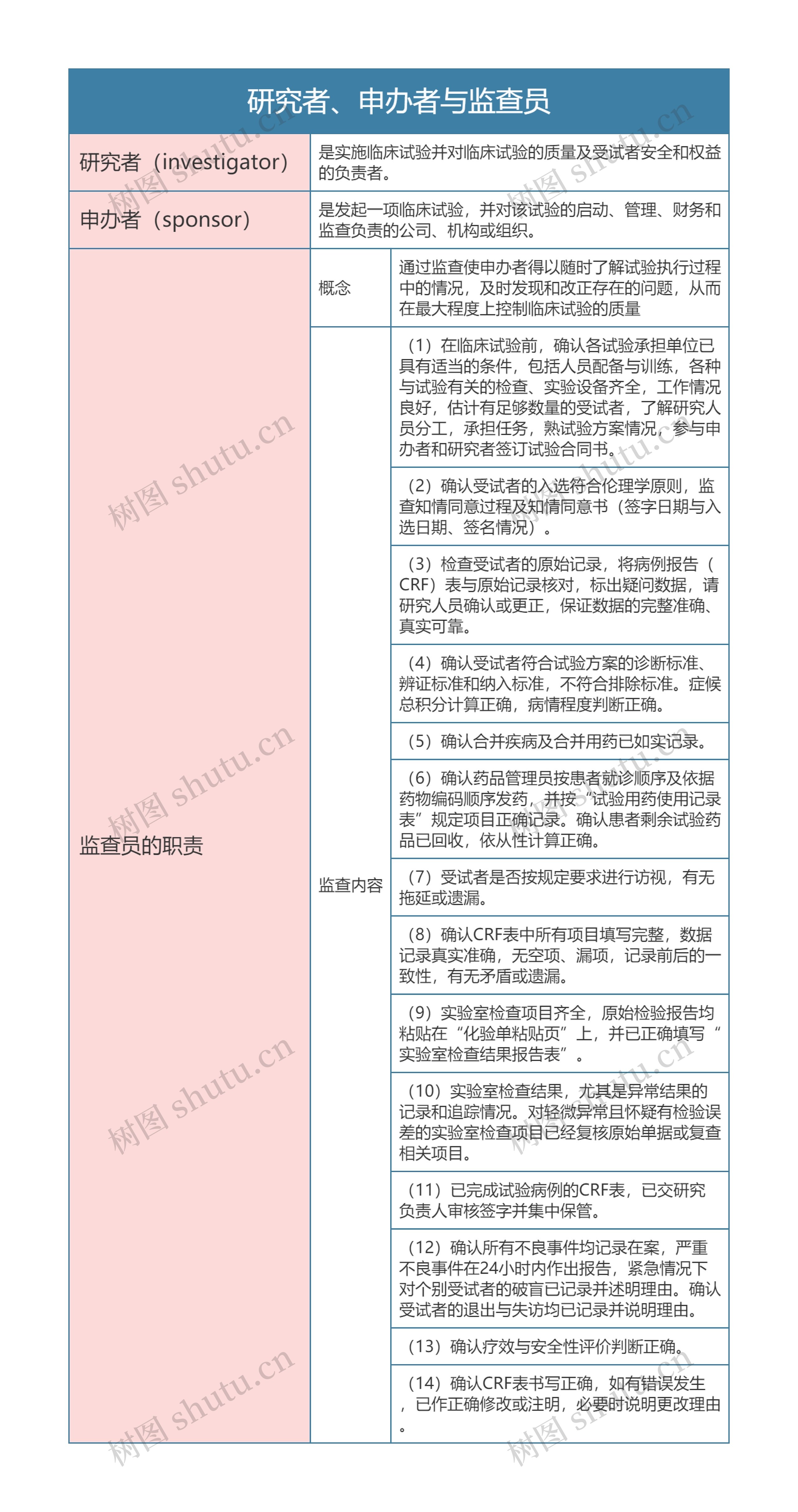
本章节主要讲述的内容是研究者、申办者与监查员等知识点归纳总结
树图思维导图提供《药理学 研究者、申办者与监查员思维导图 》在线思维导图免费制作,点击“编辑”按钮,可对《药理学 研究者、申办者与监查员思维导图 》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:bd3ccfa8a49460815f1e5776fa98fa07
思维导图大纲
相关思维导图模版
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

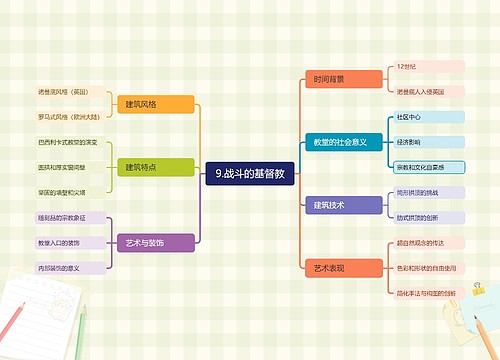
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a