人类免疫缺陷病毒的感染方式思维导图
多情又困苦
2023-02-23
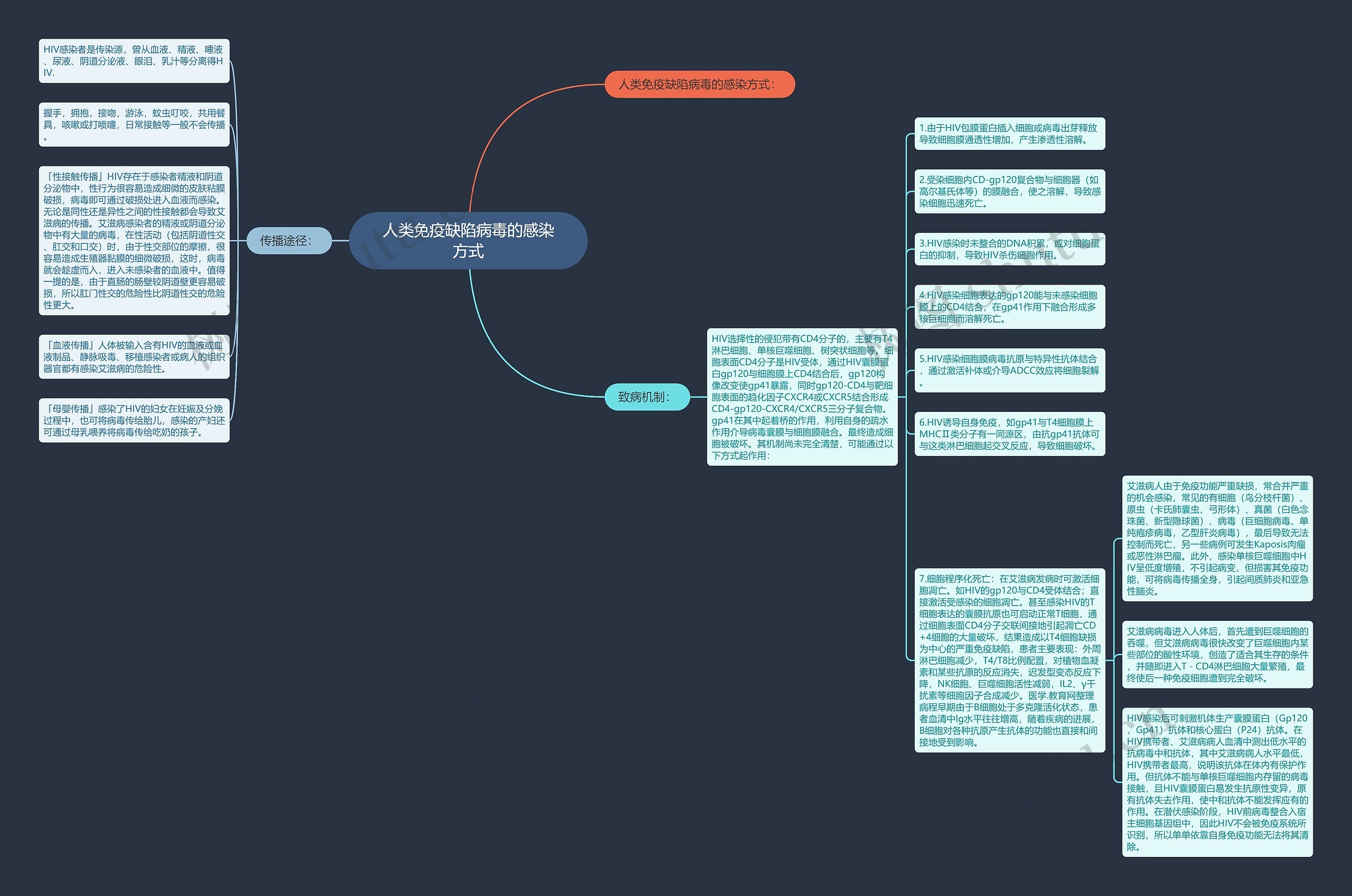
人类免疫缺陷病毒的感染方式: 传播途径: HIV感染者是传染源,曾从血液、精液、唾液、尿液、阴道分泌液、眼泪、乳汁等分离得HIV. 握手,拥抱,接吻,游泳,蚊虫叮咬,共用餐具,咳嗽或打喷嚏,日常接触等一般不会传播。
树图思维导图提供《人类免疫缺陷病毒的感染方式》在线思维导图免费制作,点击“编辑”按钮,可对《人类免疫缺陷病毒的感染方式》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:43ae4805f8af7794170d504731650d1d
思维导图大纲
相关思维导图模版
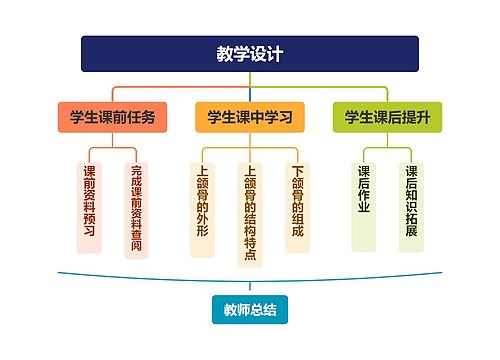
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

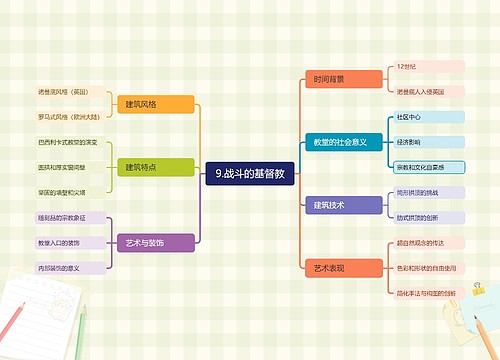
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a