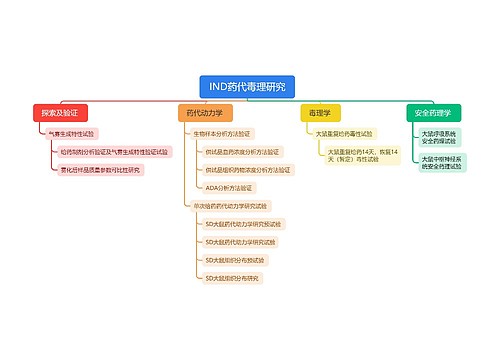
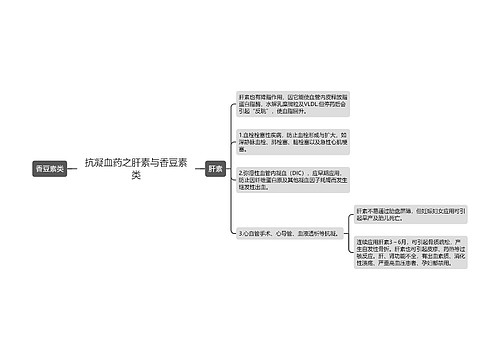
影响心功能的生理因素思维导图
我有一颗少女心耶
2023-02-21

1.交感神经系统激活 这是CHF发病过程中早期的代偿机制,是一种快速调节。患者交感神经活性增高,血中去甲肾上腺素浓度升高,从而使心肌收缩性增高,心率加快,血管收缩以维持血压,这都起到代偿作用。久后心肌氧耗量增加,后负荷增加,心工作加重,反使病情恶化,形成恶性循环。
树图思维导图提供《影响心功能的生理因素》在线思维导图免费制作,点击“编辑”按钮,可对《影响心功能的生理因素》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:00981916de2a88c85c83e723c88701b2
思维导图大纲
相关思维导图模版
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

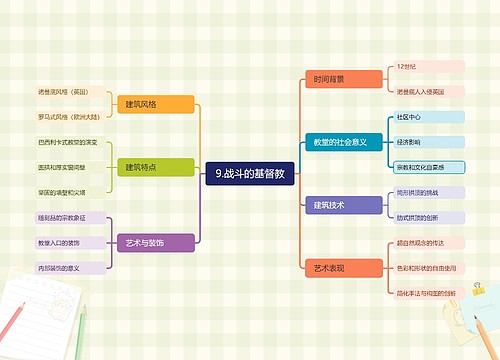
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a