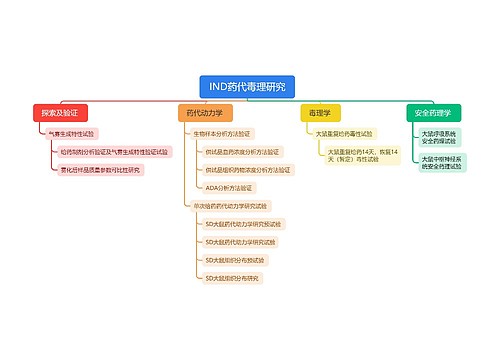
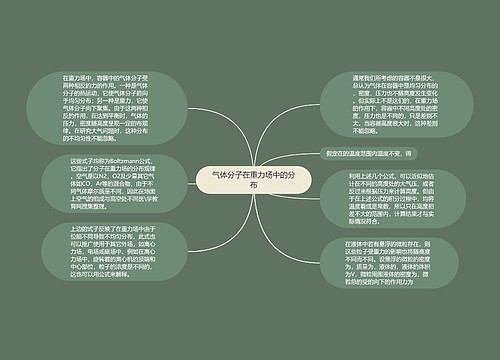
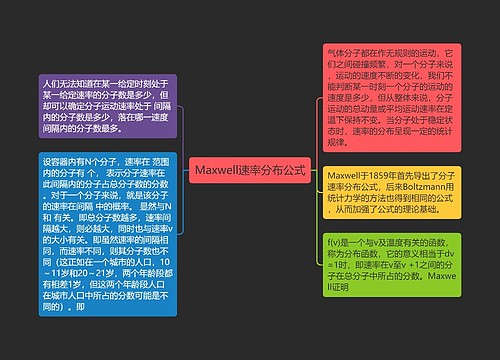
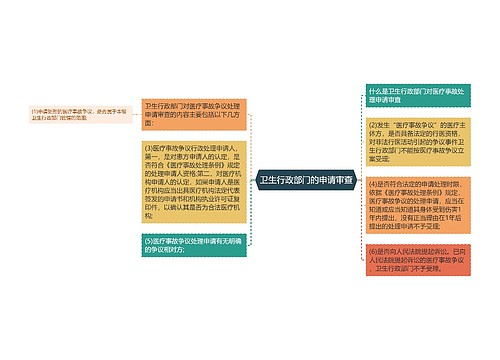
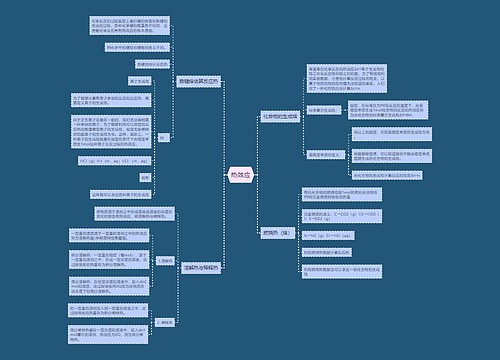
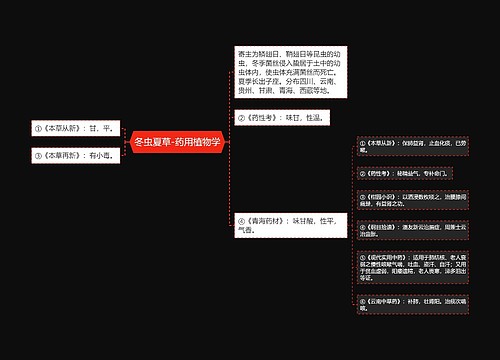
分子的平均自由程思维导图
饮尽岁月
2023-02-21

分子以很高的速度做无规则运动,它们彼此不断地相互碰撞。研究气体分子的碰撞过程,对了解气体的扩散、热传导、黏滞现象以及气相反应的速率等均具有重要的意义。 在分子的每两次连续碰撞之间所经过的路程叫做自由程(freepath)。自由程也是在不断地无规则地改变着,其平均值叫做平均自由程(maenfreepath),用表示。
树图思维导图提供《分子的平均自由程》在线思维导图免费制作,点击“编辑”按钮,可对《分子的平均自由程》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:e4975cb64cb5d988ba55b2132cb448dd
思维导图大纲
相关思维导图模版
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

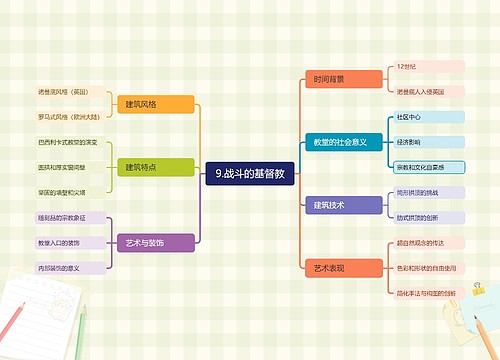
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a