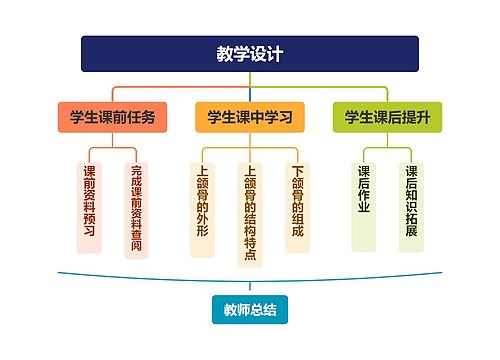
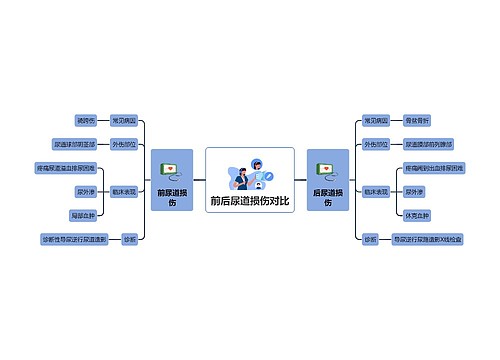
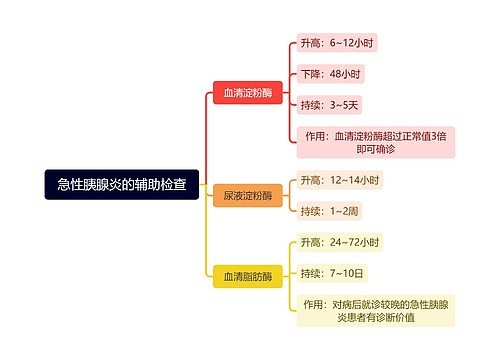
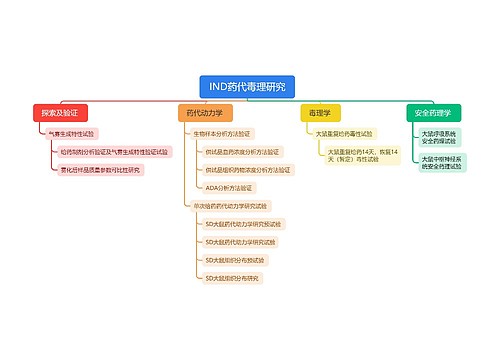
联合疫苗临床前和临床研究技术指导原则思维导图
谎话最甜
2023-02-21

前言 联合疫苗是指含有二个或多个活的、灭活的生物体或者提纯的抗原,由生产者联合配制而成,用于预防多种疾病或由同一生物体的不同种或不同血清型引起的疾病。如果将载体疫苗和偶联疫苗的载体菌或偶联的载体成分所引起的疾病也作为其适应症时,则载体疫苗和偶联疫苗也属于联合疫苗。
树图思维导图提供《联合疫苗临床前和临床研究技术指导原则》在线思维导图免费制作,点击“编辑”按钮,可对《联合疫苗临床前和临床研究技术指导原则》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:314890ddb541ceba84e12cd77ee124f4
思维导图大纲
相关思维导图模版
一、研究内容思维导图
 U682687144
U682687144树图思维导图提供《一、研究内容》在线思维导图免费制作,点击“编辑”按钮,可对《一、研究内容》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4f21797dd3e8b08f1951dfc24e7be94f
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc