药品安全性更新报告撰写规范思维导图
情书
2023-02-21

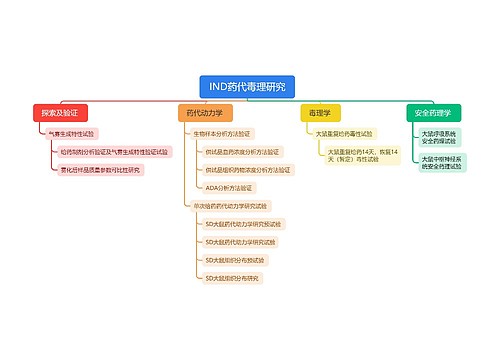
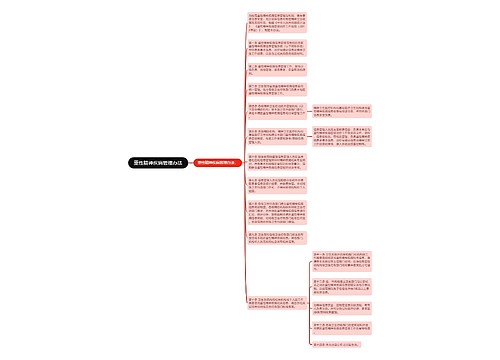
药品安全性更新报告撰写规范: 一、前言 本规范是指导药品生产企业起草和撰写《定期安全性更新报告》的技术文件,也是药品不良反应监测机构评价《定期安全性更新报告》的重要依据。
树图思维导图提供《药品安全性更新报告撰写规范》在线思维导图免费制作,点击“编辑”按钮,可对《药品安全性更新报告撰写规范》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:74327cfcb1111dad7e21fb3a0561c8b6
思维导图大纲
相关思维导图模版
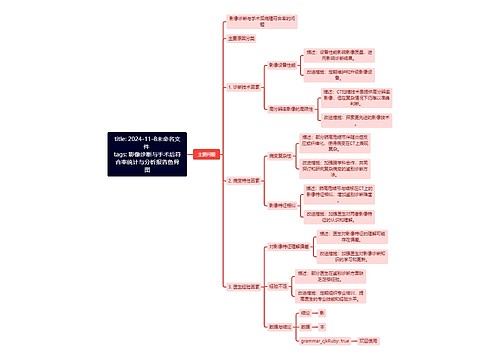
title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图思维导图
 U880271396
U880271396树图思维导图提供《title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图》在线思维导图免费制作,点击“编辑”按钮,可对《title: 2024-11-8未命名文件 tags: 影像诊断与手术后符合率统计与分析报告鱼骨图》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:f19c198bf7435acf7735ee5051a89d7b
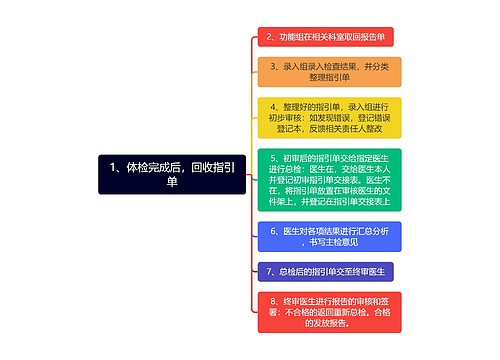
1、体检完成后,回收指引单思维导图
 U156383470
U156383470树图思维导图提供《1、体检完成后,回收指引单》在线思维导图免费制作,点击“编辑”按钮,可对《1、体检完成后,回收指引单》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:b81adb39f9ac84252ecf410072cd8287