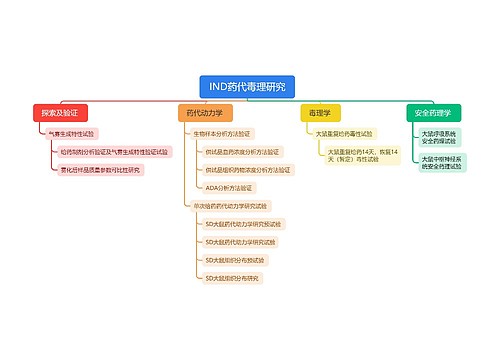
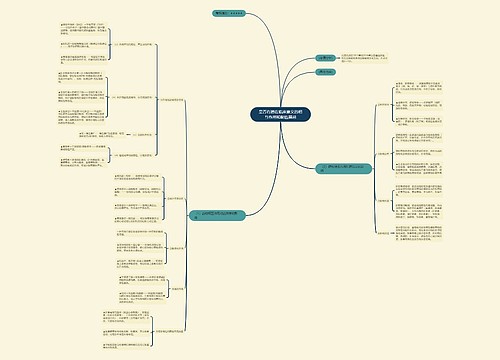
《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》解读思维导图
深知他心
2023-02-20
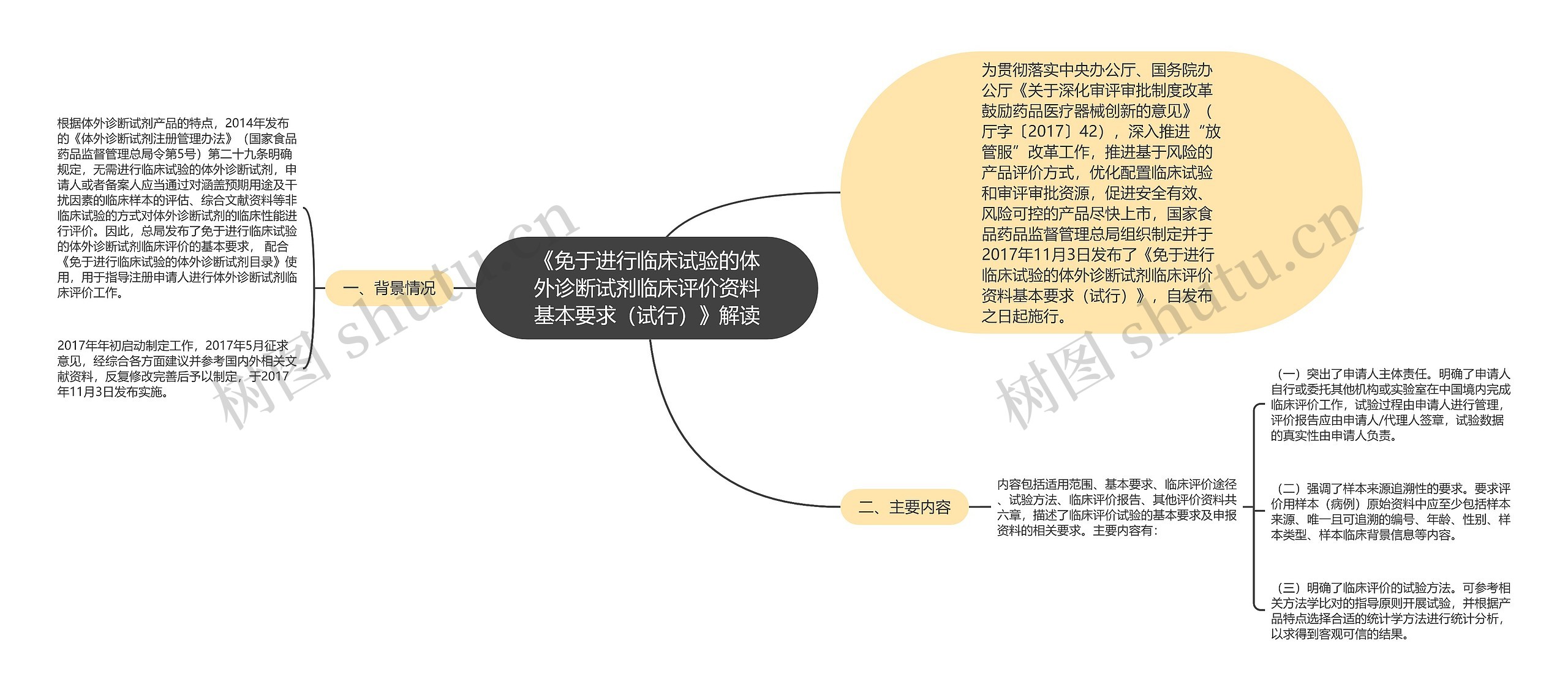
为贯彻落实中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42),深入推进“放管服”改革工作,推进基于风险的产品评价方式,优化配置临床试验和审评审批资源,促进安全有效、风险可控的产品尽快上市,国家食品药品监督管理总局组织制定并于2017年11月3日发布了《免于进行
树图思维导图提供《《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》解读》在线思维导图免费制作,点击“编辑”按钮,可对《《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》解读》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:842ce8f27b0976891c7d4b84b33ed854
思维导图大纲
相关思维导图模版
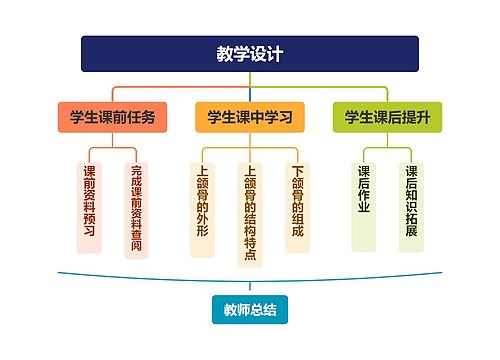
一、研究内容思维导图
 U682687144
U682687144树图思维导图提供《一、研究内容》在线思维导图免费制作,点击“编辑”按钮,可对《一、研究内容》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4f21797dd3e8b08f1951dfc24e7be94f
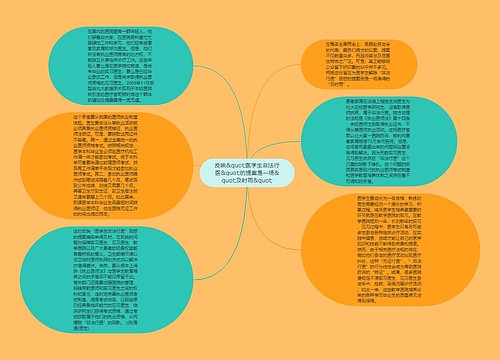
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc