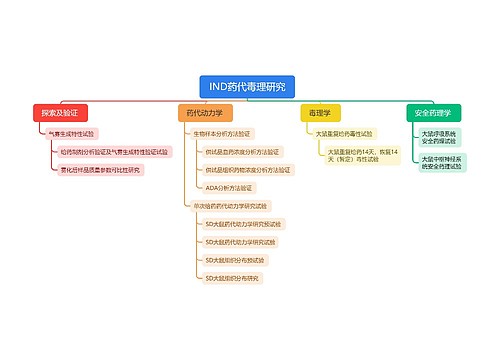
世界范围内被忽视的药品开发和获准数大增思维导图
橘味猫
2023-02-17

所谓“被忽视”的药品,指的是针对罕见病用药,因为患者人群数有限,市场规模可想而知。根据一项新的研究:过去几年中,世界范围获准用于对付以往被忽视的许多疾病的新药数比前10年开始时几乎增加了一倍。
树图思维导图提供《世界范围内被忽视的药品开发和获准数大增》在线思维导图免费制作,点击“编辑”按钮,可对《世界范围内被忽视的药品开发和获准数大增》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:9cdff634b49a531f79f25a08b03acfb7
思维导图大纲
相关思维导图模版
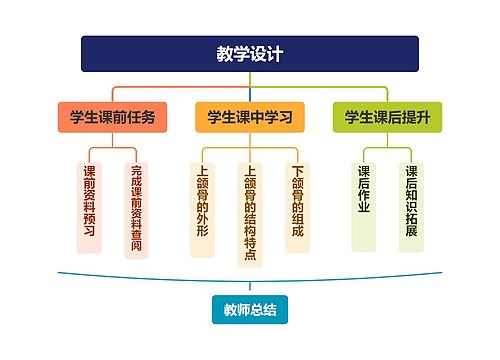
904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查思维导图
 U633687664
U633687664树图思维导图提供《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》在线思维导图免费制作,点击“编辑”按钮,可对《904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

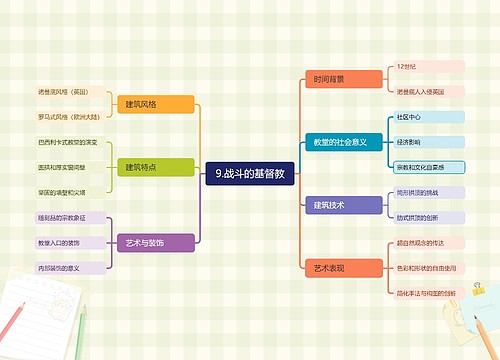
9.战斗的基督教思维导图
 U582679646
U582679646树图思维导图提供《9.战斗的基督教》在线思维导图免费制作,点击“编辑”按钮,可对《9.战斗的基督教》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a