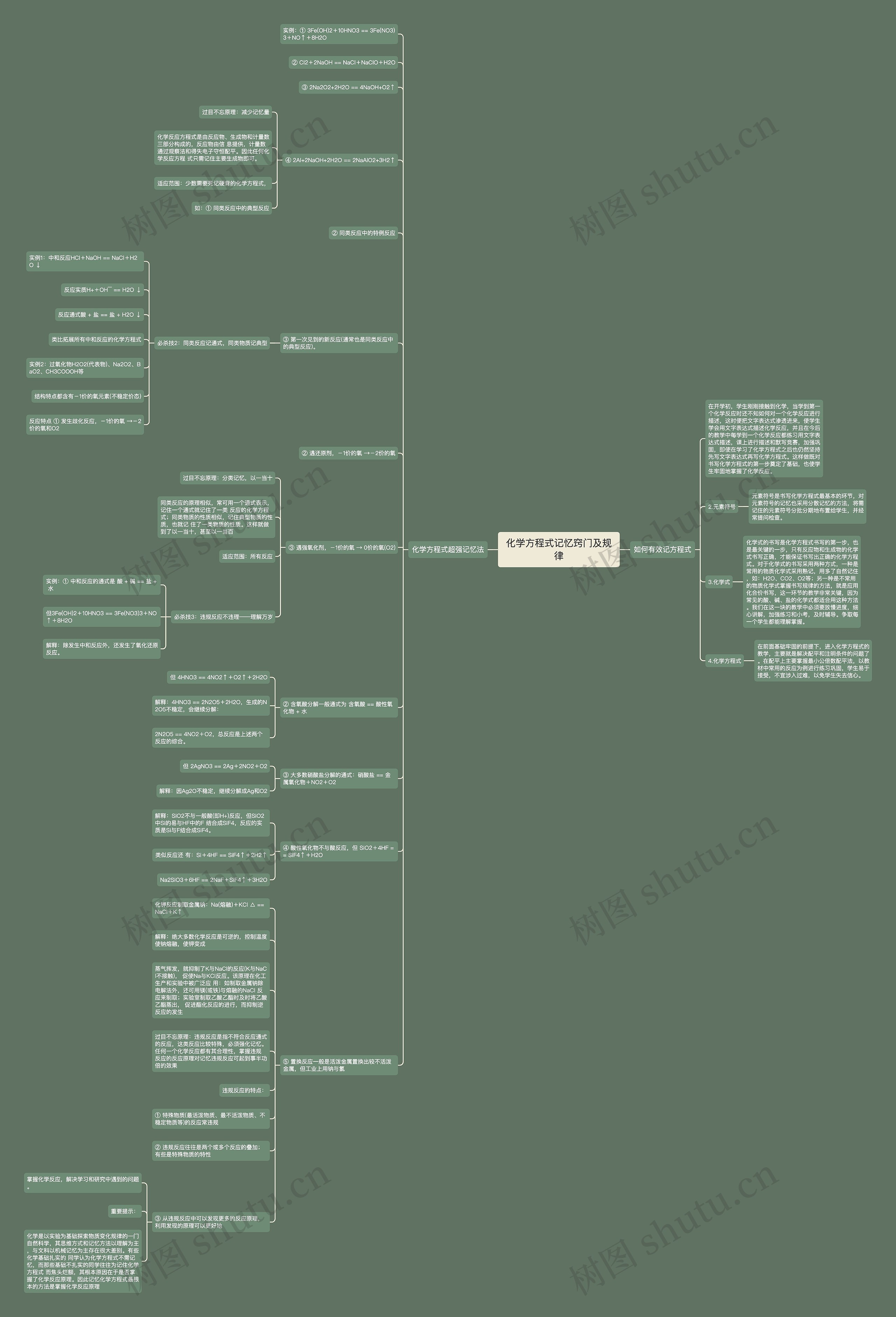
实例:① 3Fe(OH)2+10HNO3 == 3Fe(NO3)3+NO↑+8H2O
② Cl2+2NaOH == NaCl+NaClO+H2O
③ 2Na2O2+2H2O == 4NaOH+O2↑
④ 2Al+2NaOH+2H2O == 2NaAlO2+3H2↑
化学反应方程式是由反应物、生成物和计量数三部分构成的,反应物由信 息提供,计量数通过观察法和得失电子守恒配平。因此任何化学反应方程 式只需记住主要生成物即可。
③ 第一次见到的新反应(通常也是同类反应中的典型反应)。
必杀技2:同类反应记通式,同类物质记典型
实例1:中和反应HCl+NaOH == NaCl+H2O ↓
实例2:过氧化物H2O2(代表物)、Na2O2、BaO2、CH3COOOH等
反应特点 ① 发生歧化反应,-1价的氧 →-2价的氧和O2
③ 遇强氧化剂,-1价的氧 → 0价的氧(O2)
同类反应的原理相似,常可用一个通式表示,记住一个通式就记住了一类 反应的化学方程式;同类物质的性质相似,记住典型物质的性质,也就记 住了一类物质的性质。这样就做到了以一当十,甚至以一当百
必杀技3:违规反应不违理——理解万岁
实例:① 中和反应的通式是 酸 + 碱 == 盐 + 水
但3Fe(OH)2+10HNO3 == 3Fe(NO3)3+NO↑+8H2O
② 含氧酸分解一般通式为 含氧酸 == 酸性氧化物 + 水
但 4HNO3 == 4NO2↑+O2↑+2H2O
解释:4HNO3 == 2N2O5+2H2O,生成的N2O5不稳定,会继续分解:
2N2O5 == 4NO2+O2,总反应是上述两个反应的综合。
③ 大多数硝酸盐分解的通式:硝酸盐 == 金属氧化物+NO2+O2
④ 酸性氧化物不与酸反应,但 SiO2+4HF == SiF4↑+H2O
解释:SiO2不与一般酸(即H+)反应,但SiO2中Si的易与HF中的F 结合成SiF4,反应的实质是Si与F结合成SiF4。
类似反应还 有:Si+4HF == SiF4↑+2H2↑
Na2SiO3+6HF == 2NaF+SiF4↑+3H2O
⑤ 置换反应一般是活泼金属置换出较不活泼金属,但工业上用钠与氯
化钾反应制取金属钠:Na(熔融)+KCl △ ==NaCl+K↑
解释:绝大多数化学反应是可逆的,控制温度使钠熔融,使钾变成
蒸气挥发,就抑制了K与NaCl的反应(K与NaCl不接触), 促使Na与KCl反应。该原理在化工生产和实验中被广泛应 用:如制取金属钠除电解法外,还可用镁(或铁)与熔融的NaCl 反应来制取;实验室制取乙酸乙酯时及时将乙酸乙酯蒸出, 促进酯化反应的进行,而抑制逆反应的发生
过目不忘原理:违规反应是指不符合反应通式的反应,这类反应比较特殊,必须强化记忆。任何一个化学反应都有其合理性,掌握违规 反应的反应原理对记忆违规反应可起到事半功倍的效果
① 特殊物质(最活泼物质、最不活泼物质、不稳定物质等)的反应常违规
② 违规反应往往是两个或多个反应的叠加;有些是特殊物质的特性
③ 从违规反应中可以发现更多的反应原理,利用发现的原理可以更好地
化学是以实验为基础探索物质变化规律的一门自然科学,其思维方式和记忆方法以理解为主,与文科以机械记忆为主存在很大差别。有些化学基础扎实的 同学认为化学方程式不需记忆,而那些基础不扎实的同学往往为记住化学方程式 而焦头烂额,其根本原因在于是否掌握了化学反应原理。因此记忆化学方程式最根本的方法是掌握化学反应原理