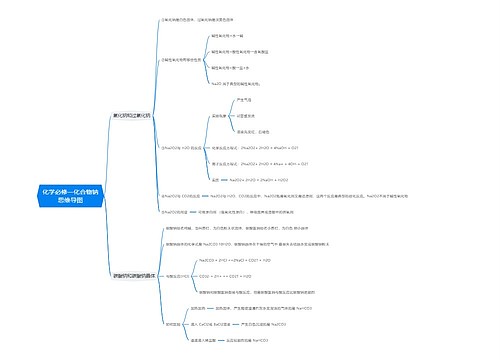
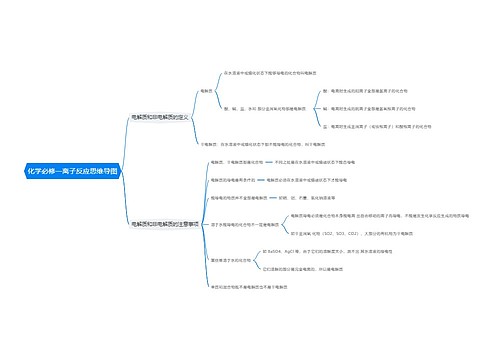
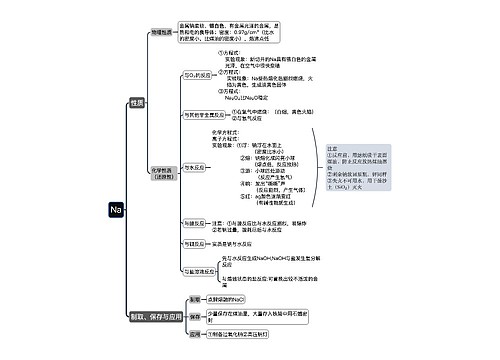
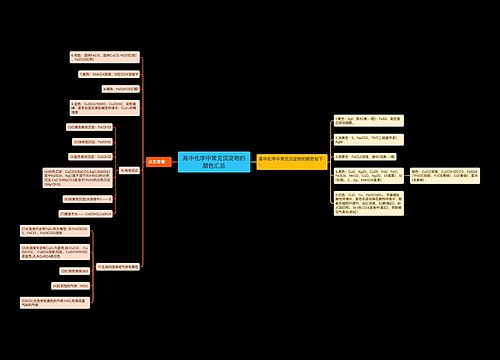
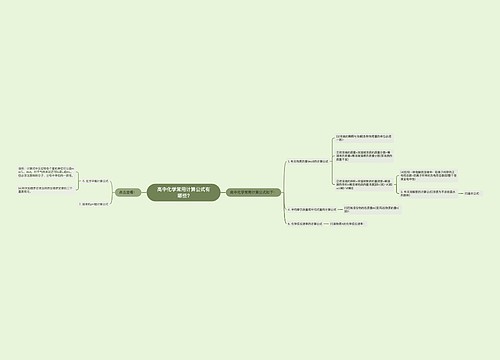
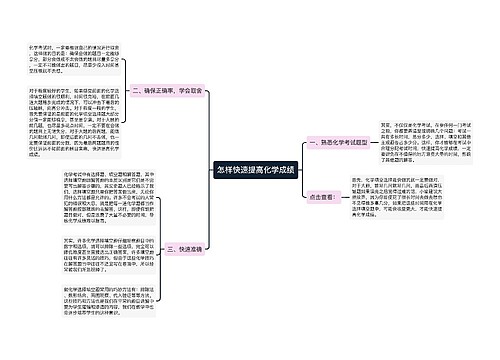
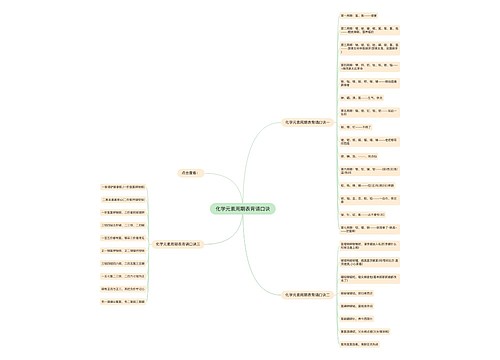
准高考生必读:化学必考知识点总结思维导图
心不动则不痛
2023-01-13

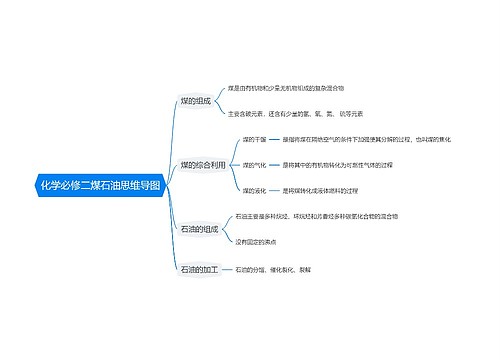
高考复习越来越紧张,高考复习资料每科都很多,那么高考化学需要掌握哪些知识点呢?高考化学是基础学科知识内容考查,下面是壹壹高考网小编为同学们整理的准高考生必读:化学必考知识点总结,供参考。
树图思维导图提供《准高考生必读:化学必考知识点总结》在线思维导图免费制作,点击“编辑”按钮,可对《准高考生必读:化学必考知识点总结》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:bab32d11029a44e79f835bceef11d455
思维导图大纲
相关思维导图模版
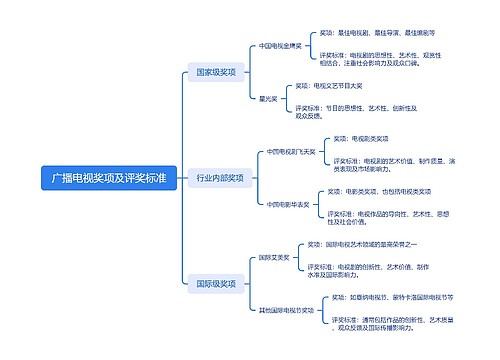
广播电视奖项及评奖标准思维导图
 U782682106
U782682106树图思维导图提供《广播电视奖项及评奖标准》在线思维导图免费制作,点击“编辑”按钮,可对《广播电视奖项及评奖标准》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a4210651fa3a78355ac9f5101bb2c616
1113爆卡会总结会会议纪要思维导图
 U245265618
U245265618树图思维导图提供《1113爆卡会总结会会议纪要》在线思维导图免费制作,点击“编辑”按钮,可对《1113爆卡会总结会会议纪要》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:aaf6c152a765d5821e8e1787f2b3226e