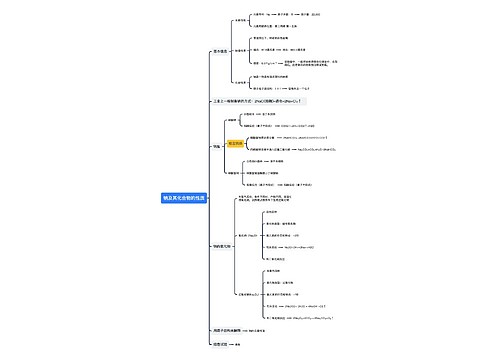
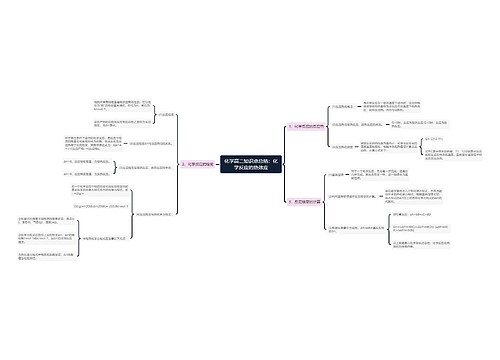
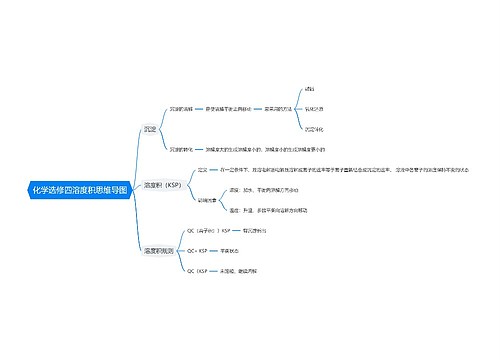
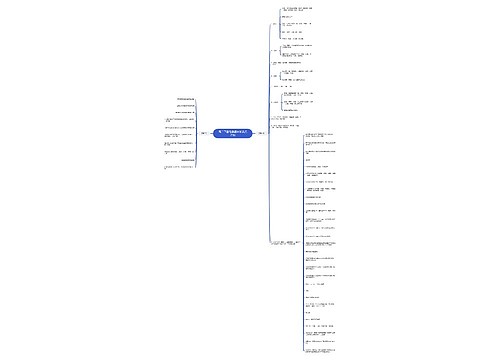
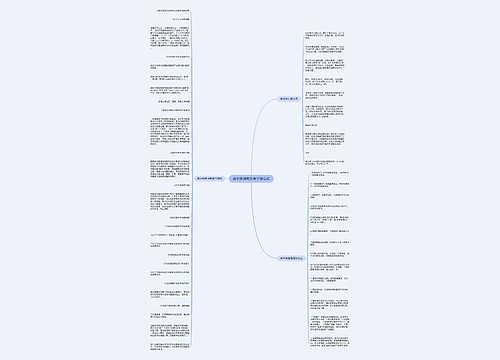
高二年级化学知识点总结思维导图
此生来迟
2022-12-21

在学习新知识的同时还要复习以前的旧知识,肯定会累,所以要注意劳逸结合。只有充沛的精力才能迎接新的挑战,才会有事半功倍的学习。树图网高二频道为你整理了《高二年级化学知识点总结》希望对你的学习有所帮助!
树图思维导图提供《高二年级化学知识点总结》在线思维导图免费制作,点击“编辑”按钮,可对《高二年级化学知识点总结》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:dc09816f27a5322efc9aa52dd0931aad
思维导图大纲
相关思维导图模版
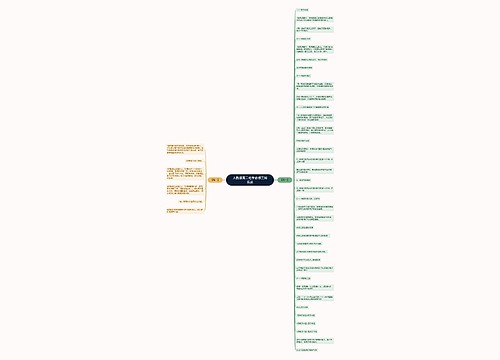
1113爆卡会总结会会议纪要思维导图
 U245265618
U245265618树图思维导图提供《1113爆卡会总结会会议纪要》在线思维导图免费制作,点击“编辑”按钮,可对《1113爆卡会总结会会议纪要》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:aaf6c152a765d5821e8e1787f2b3226e
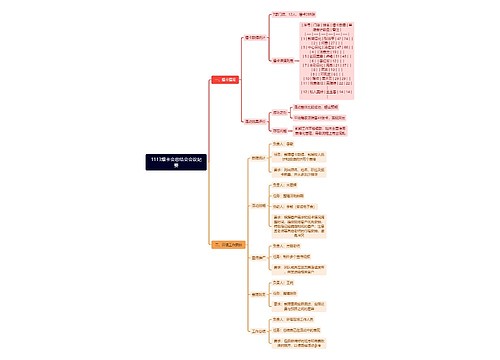
第1章 化工设计基本知识思维导图
 U882667602
U882667602树图思维导图提供《第1章 化工设计基本知识》在线思维导图免费制作,点击“编辑”按钮,可对《第1章 化工设计基本知识》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:70ec0519ed26419068a32a511862aadd