中考化学复习知识点:火眼金睛思维导图
眼眶很热
2023-04-11
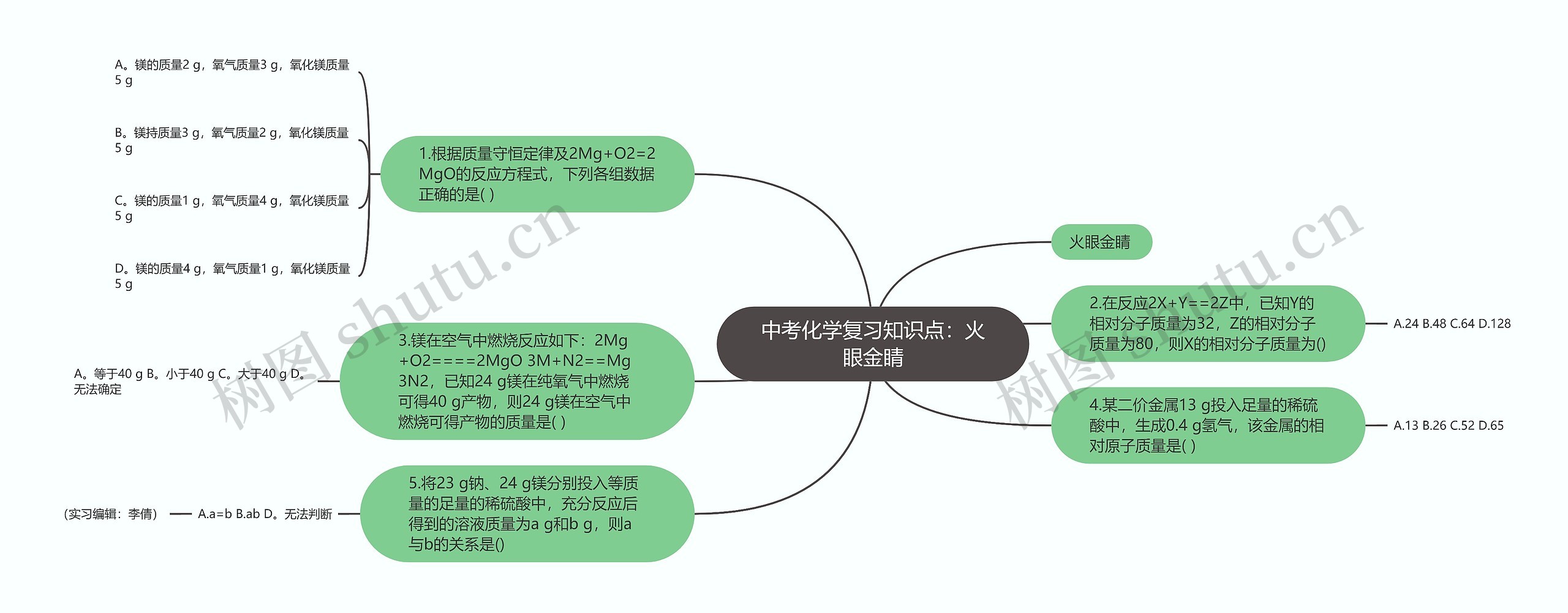
新东方中考网为广大中考生整理了中考化学复习知识点:火眼金睛,供大家参考学习。
树图思维导图提供《中考化学复习知识点:火眼金睛》在线思维导图免费制作,点击“编辑”按钮,可对《中考化学复习知识点:火眼金睛》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:e7646ca5210fa620364ce2511ac15485

新东方中考网为广大中考生整理了中考化学复习知识点:火眼金睛,供大家参考学习。
树图思维导图提供《中考化学复习知识点:火眼金睛》在线思维导图免费制作,点击“编辑”按钮,可对《中考化学复习知识点:火眼金睛》进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:e7646ca5210fa620364ce2511ac15485